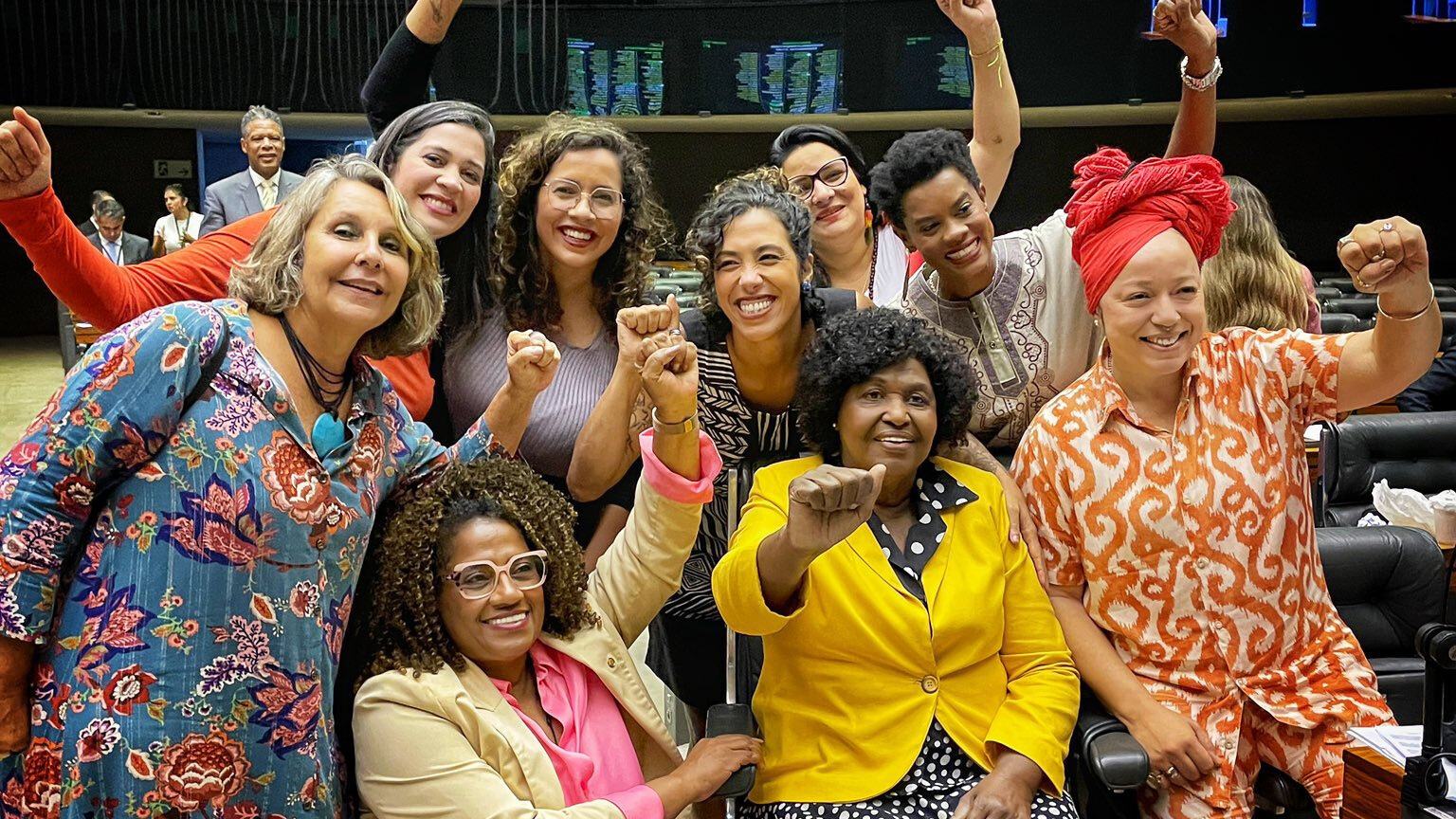Deputados aprovam autorização para produção e comércio de remédios para emagrecer

Em votação simbólica, deputados aprovaram nesta terça-feira (20), emenda do Senado ao Projeto de Lei 2431/11, que autoriza a produção, a comercialização e o consumo, sob prescrição médica, dos anorexígenos sibutramina, anfepramona, femproporex e mazindol. A matéria, agora, irá à sanção presidencial.
De acordo com a emenda do Senado, os medicamentos listados, utilizados para emagrecer, deverão ser prescritos em receituário “azul” ou “B”, usado pelo médico para indicar remédios controlados.
Para a líder do PCdoB na Câmara, deputada Alice Portugal (BA), não é “proibindo um medicamento que se coíbe a banalização de seu uso”. “Houve uma tentativa de banir um medicamento do mercado. Não podemos abrir mão da ciência, mas não é proibindo um medicamento que iremos coibir sua comercialização. Foi o que aconteceu com a sibutramina. Foi proibida e passou a ser vendida ilegalmente. É melhor que seja legalizada e que os médicos analisem caso a caso”, defendeu a parlamentar.
Polêmica antiga
O tema tem sido tratado pela Agência Nacional de Vigilância Sanitária (Anvisa) e pelo Congresso desde 2011. Naquele ano, a agência publicou a Resolução 52/11 que proibia a venda de inibidores de apetite.
A Anvisa justificou a decisão com base na análise de mais de 170 estudos relacionados aos medicamentos, concluindo que não havia comprovação de diminuição do peso corporal com seu uso, além de aumento de risco cardiovascular entre os usuários.
A venda voltou a ser liberada depois que deputados e senadores aprovaram, em 2014, um projeto publicado como Decreto Legislativo 273/14 para suspender a proibição da Anvisa.
Nova decisão
Após o decreto legislativo, a Anvisa publicou nova decisão (Resolução 50/14) com um regulamento técnico sobre o assunto, prevendo que as empresas interessadas em comercializar medicamentos contendo mazindol, femproporex e anfepramona deverão requerer novo registro à agência, cuja análise técnica levará em consideração a comprovação de eficácia e segurança dos produtos.
Segundo a norma, as farmácias só poderão manipular esses medicamentos quando houver algum produto registrado na Anvisa. Quando as substâncias tiverem registro, tanto o produto manipulado quanto o produto registrado passarão a ter o mesmo controle da sibutramina.
Já a produção industrial e a manipulação da sibutramina continuam permitidas. Porém, o regulamento mantém o mesmo controle já definido para a comercialização da substância, com retenção de receita, assinatura de termo de responsabilidade do prescritor e do termo de consentimento pós-informação por parte do usuário.
*Com informações da Agência Câmara